AAP « Tremplin ERC » – I-SITE MUSE – 2021
Investigating cell fusion and parasexual recombination in transmissible cancers – FUSCANCER
Financement : 99 k€
PORTEUSE DE PROJET
Erika Burioli (TREV)
RESUME DU PROJET
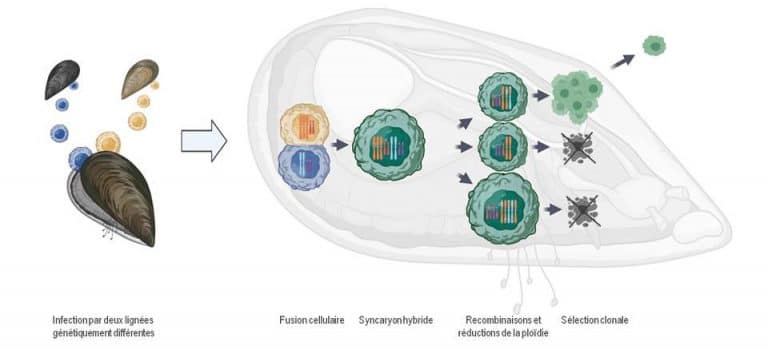
Les cellules cancéreuses mutent à mesure qu’elles se divisent, et la sélection darwinienne trie les génotypes ayant une meilleure capacité à se répliquer, à métastaser, à échapper à la réponse immunitaire ou à résister aux thérapies. Parmi les mécanismes pouvant promouvoir la variabilité génétique et phénotypique des tumeurs, des phénomènes de fusion cellulaire ont été décrits. La course évolutive est d’ordinaire stoppée par la mort ou la guérison de l’hôte mais chez quelques espèces animales des cancers ont acquis la capacité de se transmettre d’un individu à un autre prolongeant cette évolution sur des temps bien plus longs. Plusieurs de ces lignées cancéreuses infectieuses ont été décrites chez les moules bleues. Mon projet FusCancer utilisera ce modèle animal avec l’objectif d’étudier l’occurrence ainsi que les conséquences de la fusion cellulaire et de la recombinaison parasexuelle dans l’évolution des capacités adaptatives des cellules cancéreuses. Toute la diversité des événements de fusion sera considérée comme les fusions entre les cellules cancéreuses et les cellules de l’hôte mais surtout, et pour la première fois in vivo, entre des génotypes différents de lignées cancéreuses. Ce projet permettra de contribuer à la compréhension de ce phénomène évolutif dans certains types de cancer.
CONTEXTE SCIENTIFIQUE ET OBJECTIFS
Au sein du microenvironnement tumoral, des fusions entre des cellules cancéreuses ou avec des cellules normales ont déjà été décrites et ont un impact sur l’apparition et l’augmentation de l’agressivité des phénotypes malins. L’étude récente conduite par Miroshnychenko et al. (2021) apporte de nouveaux éléments à la compréhension de ces phénomènes en décrivant un nouvel aspect des fusions cellulaires entre génotypes différents : le mécanisme de recombinaison parasexuelle. Des fusions et recombinaisons entre des lignées différentes bien établies peuvent combiner des mutations qui ont été acquises durant des trajectoires évolutives indépendantes et avoir des conséquences majeures par rapport à de simples duplications du génome ou des fusions entre des cellules du même clone cancéreux.
Dans l’immense majorité des cas la course évolutive d’un cancer s’arrête toutefois avec la mort ou la guérison de l’hôte. A ce schéma quasi général, il existe quelques exceptions tout à fait spectaculaires. En effet, il existe dans la nature des cancers qui sont parvenus à contourner ce cul de sac évolutif, en acquérant la capacité de se transmettre d’un individu à un autre prolongeant cette évolution sur des temps bien plus longs. Ces cellules sont plus que de simples cancers, ce sont des organismes unicellulaires fascinants : des parasites avec un génome apparenté à celui de leur hôte. Ces formes de vie singulières pourraient représenter des modèles de choix pour améliorer notre compréhension de l’évolution somatique. En particulier, le modèle du cancer transmissible des moules, que nous étudions depuis 2017, nous offre la possibilité d’accéder à plusieurs lignées et sous-lignées cancéreuses et de reproduire expérimentalement une configuration épidémiologique réaliste puisque certaines de ces sous-lignées partagent le même environnement. Nos analyses génétiques préliminaires nous indiquent déjà que des fusions et des recombinaisons se produisent. Grâce aux efforts investis dans la maîtrise d’un procédé permettant de transmettre expérimentalement la maladie à des générations d’hôtes successives, nous pourrons étudier l’évolution des cellules issues de la fusion in vitro et in vivo sur des durées relativement longues. Le projet FusCancer représente donc une excellente opportunité d’approfondir l’étude de la fréquence, des modalités et des conséquences de la fusion et de la recombinaison parasexuelle entre des lignées cancéreuses génétiquement différentes ou avec des cellules de l’hôte.
Les résultats de FusCancer nous permettront ainsi de consolider notre dossier pour le dépôt d’une « ERC starting Grant » (LS8) en 2022.
ORGANISATION DU PROJET ET MOYENS
Durée du projet: octobre 2021-mars 2023
Le premier objectif du projet est de caractériser des événements de recombinaison par l’analyse de génomes complets de lignées cancéreuses des moules. Ce premier volet nous permettra également de développer des sondes moléculaires utilisées dans les volets successifs. Nous nous intéresserons ensuite à la fréquence et aux modalités de fusions cellulaires durant le développement des cancers transmissibles. Nous caractériserons les fusions cellulaires associées au cancer par la mise en place: i) d’un protocole nous permettant de garantir une disponibilité constante de lignées de cellules cancéreuses; ii) de protocoles de cell-tracking (long-term cell trackers cytoplasmiques, sondes moléculaires) nous permettant d’identifier les phénomènes de fusion in vivo et in vitro et de suivre le devenir de ces cellules hybrides. Enfin, nous étudierons les recombinaisons génétiques chez les cellules hybrides issues des tests in vivo à travers l’utilisation d’une puce à ADN spécifique et de whole genome sequencing.
Le projet FusCancer est un projet pluridisciplinaire qui allie des aspects de biologie cellulaire et moléculaire et de génomique évolutive. Cette complémentarité disciplinaire est assez originale sur le site montpelliérain et correspond à une combinaison émergente gagnante entre l’IHPE et l’ISEM soutenue par MUSE.
Plusieurs membres permanents de l’IHPE sont également impliqués dans le projet : Delphine Destoumieux-Garzon, Guillaume Charrière, Gaëlle Courtay, Juliette Pouzadoux; ainsi que des membres de l’ISEM : Nicolas Bierne, Emilie Le Goff, Stephen Baghdiguan et Nelly Godefroy.
Nous collaborerons aussi avec le Pacific Northwest Research Institute à Seattle, USA (Michael Metzger) et le College of Life and Environmental Sciences et l’University of Exeter, UK (Robert Ellis).